Химия

Химические связи
План урока:
Внутримолекулярные взаимодействия
Металлическая химическая связь
Межмолекулярные взаимодействия
Химические связи – это основа окружающего мира. Катион натрия Na+и анион хлора Cl-поодиночке не играют такой важной роли, как результат их взаимодействия хлорид натрия NaCl. Это соединение придает еде соленый вкус, а также является физраствором в медицинских капельницах.
Химическая связь формируется с помощью воздействия атомов друг на друга. В итоге создаются молекулы, ионы и радикалы. Она обуславливается взаимоотношениями частиц, имеющих заряд. Химическая связь определяет стабильность кристалла.
В одном и том же соединении иногда встречаются разные связи.
- Основания. В гидроксидной группе формируется ковалентная полярная связь, а между этой группой и металлом – ионная.
- Соли кислот, содержащих кислород. Полярная связь формируется между неметаллом и кислородом, а ионная – между металлом и остатком кислоты.
- Соли аммония. Между азотом и водородом образуется полярная связь, между ионами аммония и остатком кислоты — ионный тип связи.
- Пероксид металлов. Неполярная связь формируется в кислороде, а ионная – между атомами металла и кислорода.
Внутримолекулярные взаимодействия
Связь в веществе формируется с помощью внешних электронов. Важное значение имеет электроотрицательность (ЭО) – сила сдерживания атомом валентных электронов.Знание электроотрицательности поможет установить вид связи.Электроотрицательность представлена в таблице Полинга. Разность ЭО влияет на формирование связи.

Ковалентная химическая связь
Ковалентная связь создается с помощью формирования совместной пары электронов. Ей характерна небольшая разность электроотрицательностей между неметаллами или внутри молекулярной структуры, сформированной одинаковыми атомами.
Ковалентная неполярная связь свойственна для равной электроотрицательности. Она встречается в одинаковых атомах. Например, два атома водорода Н создают молекулу Н2. Полярная связь встречается у атомов с разницей ЭО в пределах 0,4-2 единиц.
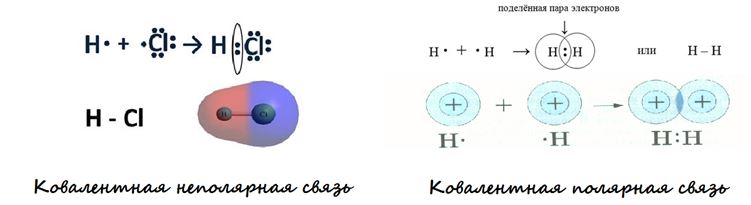
К важнейшим свойствам ковалентной связи относятся:
- направленность (строение и форма соединения);
- насыщаемость (создание определенного числа связей);
- полярность (распределение плотности внутри молекулы);
- поляризуемость (смещение общих электронов в одну из сторон).
Ковалентная связь может формироваться посредством донорно-акцепторного или обменного механизма. В первом случае электронная пара для связи есть у одного атома. Во втором случае оба атома образуют связь.

Ковалентная неполярная связь
Молекула водорода H2 сформирована из двух атомов с равной электроотрицательностью. На единственном уровне находится по одному электрону. Для данной молекулы есть одна совместная пара электронов. Т.к. у атомов одинаковая электроотрицательность, электроны никуда не смещаются.

Без ковалентной связи на Земле могла бы не зародиться жизнь. Кислород О2 образуется с помощью неполярной связи. Кислород участвует в процессах дыхания человека и животных, используется в реакциях горения, а также служит катализатором на некоторых производствах. Но в результате неполярной связи создаются не только полезные, но и вредные молекулы. Например, газ хлор Cl2. Это токсичный удушающий газ, который вызывает ожоги легочной ткани. Хлор использовался Германией в качестве химического отравляющего вещества во времена Первой мировой войны.
Ковалентная полярная связь
Полярная связь появляется с разностью ЭО в 0,4-2 единиц. В таких соединениях электронная плотность смещается к более электроотрицательному. Более электроотрицательному атому свойственен частично отрицательный заряд δ-, а менее – частично положительный заряд δ+.
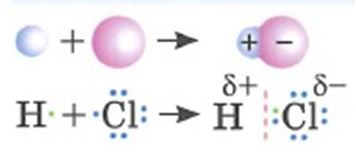
Полярная связь прочнее, чем неполярная. Это можно объяснить тем, что силы притяжения есть именно в полярных молекулах. Полярность определяет характеристики соединения. От нее зависит ход реакций и способность соседствующих связей вступать в различные взаимодействия.
Ковалентные полярные связи есть внутри человеческого организма. В желудке сильнокислая среда, которая образуется за счет соляной кислоты HCl. Она осуществляет кислотную денатурацию белковых структур, способствует разбуханию пищевых веществ, оказывает бактерицидное действие на микробов, поступающих в желудок. Также с помощью ковалентной полярной связи создается молекула воды H2O. Без воды не было бы жизни на нашей планете. В ней протекают основные процессы жизнедеятельности. Как известно, наличие воды определило начало жизни на Земле. Ученые в поисках жизни на других планетах ищут именно водную среду.
Ионная химическая связь
Ионную связь невозможно создать без электростатического притяжения. Она характерна для ионов – атомов, которые образуются при удалении или принятии электронов. Ионная связь, как правило, присутствует в веществах между металлами и неметаллами. Разница в электроотрицательностях должна быть более 2-х единиц.
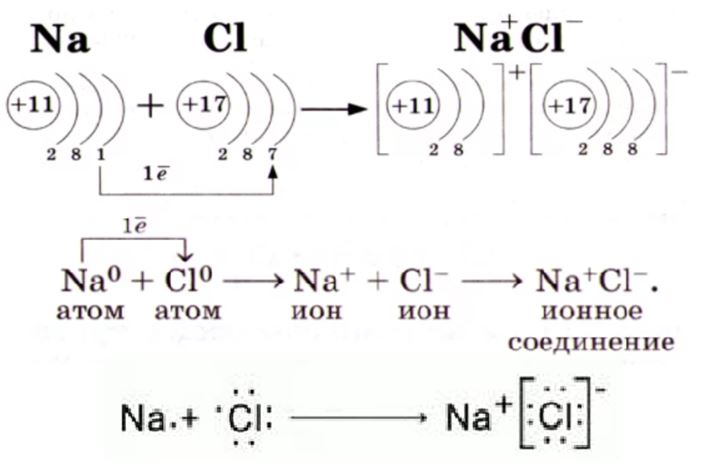
В отличие от ковалентной в ионной связи осуществляется перенос электронов и атомы приобретают положительный или отрицательный заряд.

Без ионной связи не существовало такого соединения как хлорид натрия NaCl. Области применения различны. Хлорид натрия используется в пищевой промышленности и медицине. Хлорид натрия в смеси с другими солями, песком или глиной используется зимой в качестве технической соли. Смесь применяется против гололеда.В организме около 5 литров крови, которые включает в среднем 0,9 % солей. Выделительная система человека в день выводит из организма 15 граммов хлорида натрия. Таким образом, без ионной связи невозможно представить жизнь на нашей планете.
Металлическая химическая связь
Металлическая связь формируется между ионами металлов. Она характеризуется образованием кристаллической решетки. Металлы характеризуются наличием на внешнем уровне 1-3 электрона. Т.о. металлы являются сильными восстановителями. Такая связь встречается в простых веществах металлах.
Металлы приобретают положительный заряд при отдаче электронов. Электроны, которые ушли от металлов, свободно передвигаются между металлическими ионами.Общие электроны удерживают катионы металлов и образуют прочную кристаллическую решетку.

В Средние века алхимики считали, что металлы определяют характер и поведение человека. Например, преобладание в организме свинца делает человека угрюмым. Повышенное количество железа создает агрессию. Научно эти предположения не доказаны, но с точностью можно сказать, что без металлов невозможно представить живой мир. Они оказывают значительное влияние на жизнь планеты.
Атомы железа Fe входят в состав гемоглобина, с помощью которого осуществляется транспорт кислорода. Кислород О2, который связан ковалентной неполярной связью, необходим в окислительно-восстановительных реакциях организма. Именно благодаря железу у человека и животных кровь имеет красный оттенок. Данный элемент в организм поступает вместе с продуктами питания – печенью, яблоками, творогами, сливами, дынями, тыквой, помидорами и абрикосами и в других овощах и фруктах. Таким образом, все металлы влияют на жизнь человека и животных.
Межмолекулярные взаимодействия
Они встречаются у атомов с нейтральным зарядом. В итоге ковалентные связи не формируются. Такие взаимоотношения определяются Ван-дар-Ваальсовыми силами.К таким взаимодействиям относятся водородные связи.
Водородная химическая связь
Водородные связи – межмолекулярные взаимодействия, в которых присутствуют поляризованные ковалентные связи.
У механизма образования электростатический и донорно–акцепторный характер. В качестве донора электронов выступает атом с высокой ЭО, а в качестве акцептора — водород. Такая связь определяет такие свойства как направленность и насыщаемость.

Сила водородной связи определяется ЭО атома, отличного от водородного атома. Например, степень взаимодействия в молекуле плавиковой кислоты HF выше, чем в аммиаке NH3. Если посмотреть на таблицу Полинга, то можно определить, что фтор очень электроотрицателен.
Наличие водородной связи меняет свойства вещества. Они создают притяжение между молекулярными структурами, что повышает температуры плавления или кипения. У многих соединений с водородными связями аномально высокие температуры кипения.
Водородная связь характерна для различных органических соединений, в том числе нуклеиновых кислот. Несмотря на низкую энергию связи, водородная связь крайне важна для жизни на Земле. За счет водородных связей образуется вторичная структура белка.
ВОПРОСЫ И ЗАДАНИЯ
Хлорид калия KCl является примером … связи
1) ионной 2) водородной 3) ковалентной полярной 4) ковалентной неполярной
Разница электроотрицательностей атомов должна составлять более 2-х единиц в соединениях с … связью
1) металлической 2) ковалентной 3) ионной 4) водородной
Ковалентная полярная связь образуется между
1) атомами металла и неметалла 2) атомами металлов 3) атомами водорода и неметалла 4) атомами неметаллов
Ионный тип связи формируется в веществах между
1) металлом и неметаллом 2) двумя металлами 3) водородом и неметаллом 4) двумя неметаллами
Электроотрицательность можно определить по таблице
1) Д.И. Менделеева 2) А.М. Бутлерова 3) Л. Полинга 4) М. Склодовской-Кюри



