Химия

Агрегатные состояния
План урока:
Области применения агрегатных состояний
В мире множество веществ, которые могут принимать разную форму. Вода в чайнике жидкая, а если начать ее кипятить, то она станет паром. Если эту же воду поставить в морозильную камеру, то она затвердевает. Вещества на нашей планете как актеры, которые могут играть разные роли.
Агрегатное состояние – принятие химическими веществами разной формы в зависимости от изменений внешней среды. Всего существует четыре состояния – газовое, жидкое, твердое, плазменное. Но к агрегатным относятся только три состояния– газ, жидкость и твердые вещества. В плазменном состоянии не сохраняется атомно-молекулярный состав вещества, а в трех других – сохраняется.
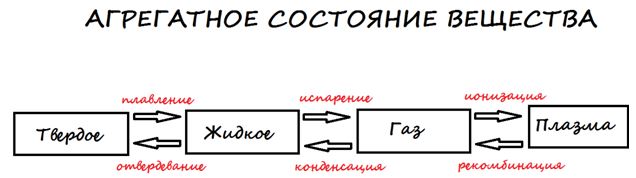
Агрегатное состояние вещества и фазовые переходы. Гуглдиск
Процесс перехода одного состояния в другое называется фазовым переходом. Он характеризуется изменением структуры связей между атомами, молекулами или ионами. Фазовый переход сопровождается поглощением или выделением теплоты. Ему сопутствуют скачкообразные изменения физических и химических свойств — плотности, растворимости и др.
Вещество изменяет агрегатное состояние при следующих условиях.
- Плавление – переход вещества из твердого состоянияв жидкое (таяние льда).
- Затвердевание – обратный плавлению процесс (зимние узоры на стекле).
- Парообразование – переход вещества из жидкого состояния вгазообразное (выделение пара из кипящего чайника).
- Конденсация – обратный парообразованию процесс (появление капель воды при принятии горячего душа).
- Сублимация, или возгонка – переход из твердого состояния в газообразное, минуя жидкую стадию(переход сухого льда в состояние углекислого газа).
- Десублимация – обратный сублимации процесс (появление инея на деревьях).
Газообразное состояние
Газ – состояние, при котором частицы вещества слабо связаны друг с другом, занимают все пространство и движутся хаотично. Расстояния между атомами и молекулами значительно превышают их размеры. Газовое состояние можно сравнить с футбольным полем, на котором быстро и независимо друг от друга передвигаются спортсмены. Футболисты, как и молекулыв газообразном состоянии, взаимодействуют только когда сталкиваются или близко подходят друг к другу.

Расположение молекул газа.
Газообразное состояние находится в виде различных запахов. У газов нет формы и объема, поэтому частицы распространяются по всему пространству. Например, запах газа из невыключеннойплиты быстро охватывает всю квартиру благодаря хаотичности движения молекул и их стремлению заполнить все помещение.
Газы обладают следующими особенными свойствами.
- Равномерность заполнения всего объема.
- Небольшая плотность при высокой скорости диффузии.
- Легкое сжатие.
Газообразноеагрегатное состояние веществаможно оценивать как насыщенный и ненасыщенный пар. Если число молекул, вылетающих из жидкости, станет равным числу молекул пара, возвращающихся в жидкость, то возникает динамическое равновесие между паром и жидкостью – состояние насыщенного пара. В ненасыщенном такого равновесия нет.
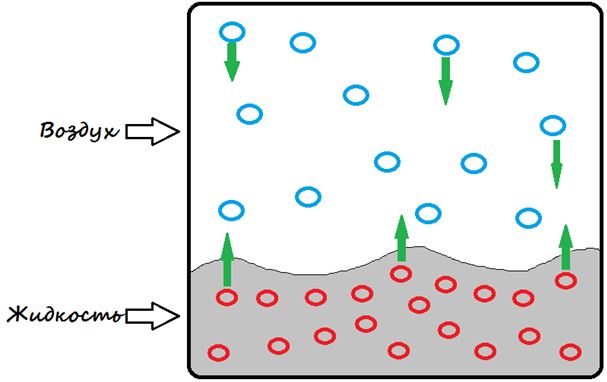
Насыщенный пар.
При нахождении жидкости в открытом сосуде, объем вещества уменьшается из-за испарения. Если поместить ту же жидкость в закрытый сосуд, объем вещества останется прежним. Сначала начнется процесс испарения и продолжается до тех пор, пока число покинувших жидкость молекул не станет равно возвратившимся назад из паров. Т.е. в закрытом сосуде возникает динамическое равновесие. Изменение внутренней энергии вещества определяется по формуле:
ΔU = ± mr, где m — масса тела, r — удельная теплота парообразования.
Переход веществиз газообразногов жидкое состояние, называется сжижением. Увеличение давления и понижение температуры приводит к уменьшению расстояний между молекулами, увеличению силы взаимодействия и превращению в жидкость. Сжижение характеризуется критической температурой. Она определяется в точке, в которой переход газа в жидкость невозможен.
Жидкое состояние
Жидкость – состояние, в котором происходит заполнение частицами всего объема. В отличие от газов, у жидкости есть поверхность. Также для нее характерно высокое межмолекулярное взаимодействие и низкая сжимаемость. Частицы в жидкости располагаются как гости, приглашенные в небольшую квартиру. Приглашенные, как и молекулы, свободно передвигаются в пространстве и ведут себя по-разному. Из-за того, что гостей много, человеку необходимо постоянно оглядываться, чтобы ни на кого не натолкнуться. Присутствующиенаходятся близко друг к другу.
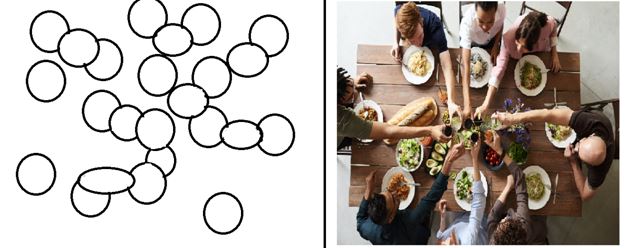
Жидкие вещества. Гуглдиск:
Жидкое агрегатное состояниеобладает особенным свойством – текучестью. Она объясняется тем, что частицы колеблются внутри квазикристаллической решетки и перемещаются между ними. Получается сложная траектория — колебания вокруг центра, перемещающегося в пространстве.
Твердое состояние
Твердому состоянию свойственна высокая степень упорядоченности частиц. Каждая молекулаколеблется около среднего положения, оставаясь жестко связанной с соседями и образуя кристаллическую решетку. Твердое агрегатное состояние напоминает воинскую часть, в которой все подчиняется строгим правилам. В строю, как и в твердых веществах, каждому солдату предоставлено определенное место. Самостоятельное перемещение внутри строя запрещается. Солдаты стоят плотно плечом к плечу, расстояния между ними маленькие. Столкновения внутри строя невозможны.

Твердые вещества.
Твердые вещества имеют форму и сохраняют свой объем. Их классифицируют на несколько видов.
- Аморфные – вещества, в которых относительно упорядоченные частицы имеют сильные ковалентные, полярные и неполярные, ионные, металлические связи.
- Кристаллические – вещества, в которых частицы расположены строго по своим местам.
Аморфные тела по свойствам напоминают жидкости,так как их молекулы передвигаются между хаотично расположенными условными центрами. Примерами аморфных веществ служат пластмассы, смолы и другие неметаллы. Примеры кристаллических тел – железо, серебро и другие металлы.
Нагревание кристаллических веществ ведет к нарушению расположения частиц и увеличению расстояний между ними. При достижении температуры плавленияпроисходит перестройка молекул, и твердое тело превращаетсяв жидкое. Количество теплоты, которое необходимо для расплавления некоторой массы веществ, подчиняется формуле:
Q = km, где k — удельная теплота плавления этого вещества, m — его масса.
Плазма
Плазма – не выдумка из фантастических фильмов и книг, а ионизированный газ. Она характеризуется одновременным присутствием нейтральных и заряженных частиц. Ионизаторы воздуха строятся на принципе перехода из газообразного вещества в плазму.

Северное сияние
Получить плазму сложно, т.к. для этого вещество необходимо нагревать до температур порядка сотен тысяч градусов и выше. Полученная смесь состоит из электронов, ядер и положительно заряженных ионов. Плазма электронейтральна, но обладает высокой проводимостью. Внутри нее происходят непрерывные разрежения и сгущения, сопровождающиеся образованием плазмоидов — упорядоченных структур правильной формы. Хотя плазма на нашей планете – редкое явление, каждый человек хотя бы раз в жизни сталкивался с ней. Плазменное состояние характерно для северного сияния и молний. В масштабах Вселенной основная масса вещества находится в виде плазмы.
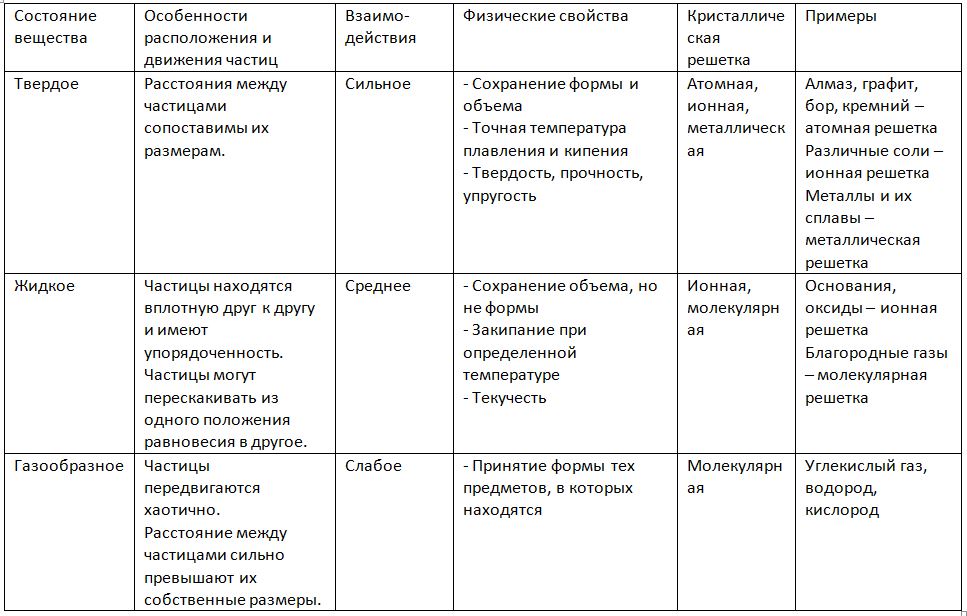
Сводная таблица агрегатных состояний
Области применения агрегатных состояний
Способность веществ переходить из одного агрегатного состояния в другой активно используется человеком. На ней основаны многие промышленные процессы.
- Способность металлов плавиться и принимать различную форму используется в черной и цветной металлургии.
- При получении соли и других химических соединений применяется выпаривание, при котором вещество получается после испарения жидкости.
- Инертные газы используются в осветительных приборах.
- Жидкий кислород применяется в медицине в качестве средства анестезии.
Таким образом, без различных агрегатных состояний невозможно было бы представить жизнь на планете. Фазовые переходы веществ используются практически во всех областях жизнедеятельности.
ВОПРОСЫ И ЗАДАНИЯ
Ионизация – процесс перехода
1) газа в жидкое состояние 2) жидкости в твердое состояние 3) газа в плазменное состояние 4) жидкости в плазменное состояние
При каком состоянии частицы располагаются дальше друг от друга?
1) газ 2) жидкость 3) твердые вещества 4) плазма
У какого агрегатного состояния есть особенное свойство – текучесть?
1) плазма 2) жидкость 3) газ 4) твердые вещества
Насыщенный пар характеризуется
1) высоким содержанием молекул газа 2) высоким содержанием молекул жидкости 3) равновесием между числом молекул газа и жидкости 4) равновесием между числом молекул газа и твердого вещества
Инертные газы используются в
1) металлургии 2) медицине 3) пищевой промышленности 4) осветительных приборах



